




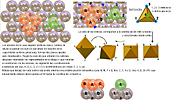


En la Naturaleza es frecuente que los dos primeros planos de aniones O y/o OH queden unidos por un catión tetraédrico, como es el caso del Si, y encima se sitúe otro plano de OH con un plano intermedio de cationes octaédricos (de Mg o de Al) que los une.
De lo anteriormente se deduce que los filosilicatos pueden ser considerados como un empaquetamiento de iones O que engloban a diversos cationes (Si, Al, Mg y H), concepto que puede ser aplicado a la Tierra en su conjunto.
En resumen, a estructura se origina por un apilamiento de planos paralelos con simetrías hexagonales, alternando los planos de aniones (O y OH) y los de cationes (Si, Al y Mg).

